برچسب گذاری سیناپسی
برچسبگذاری سیناپسی ، یا فرضیه برچسبگذاری سیناپسی، برای توضیح اینکه چگونه سیگنالدهی عصبی در یک سیناپس خاص، هدفی برای انتقال محصول مرتبط با پلاستیسیته (PRP) بعدی برای LTP و LTD پایدار ایجاد میکند، پیشنهاد شده است. اگرچه هویت مولکولی تگ ها ناشناخته باقی مانده است، مشخص شده است که آنها در نتیجه تحریک فرکانس بالا یا پایین تشکیل می شوند، با PRP های ورودی تعامل می کنند و طول عمر محدودی دارند. [۱]
تحقیقات بیشتر نشان میدهد که محصولات مرتبط با پلاستیسیته شامل mRNA و پروتئینهایی از شفت سوما و دارینهیک هستند که باید توسط مولکولهای درون ستون فقرات دارینهیک برای دستیابی به LTP و LTD پایدار جذب شوند. این ایده در فرضیه برچسب و تسخیر سیناپسی بیان شد. به طور کلی، برچسبگذاری سیناپسی در مورد زیربنای مولکولی چگونگی تولید L-LTP و منجر شدن آن به تشکیل حافظه توضیح میدهد.
تاریخچه[ویرایش]
فری، محققی در مؤسسه نوروبیولوژی لایبنیتس (بعدها در کالج پزشکی جورجیا و دانشگاه لوند)، و موریس، محققی در دانشگاه ادینبورگ ، [۲] اساس فرضیه برچسبگذاری سیناپسی را پایهریزی کردند و بیان می کنند:
"ما پیشنهاد می کنیم که LTP فرایند ایجاد یک "برچسب سیناپسی" مستقل از تلفیق پروتئین و کوتاه مدت را در سیناپس تقویت شده آغاز کند که پروتئین(های) مربوطه را برای ایجاد LTP دیررس جدا می کند. در حمایت از این ایده، اکنون نشان می دهیم که تحریک کزازی ضعیف، که معمولاً فقط به LTP اولیه یا تتانیزاسیون مکرر در حضور مهارکنندههای تلفیق پروتئین منجر میشود، که هر کدام منجر به LTP دیرهنگام وابسته به تلفیق پروتئین، با تتانیزاسیون مکرر در ورودی دیگری به همان جمعیت نورون ها اعمال شده است. این یافته ها نشان می دهد که تداوم LTP نه تنها به رویدادهای محلی بستگی دارد القای آن، بلکه بر روی فعالیت قبلی نورون نیز بستگی دارد." [۲]
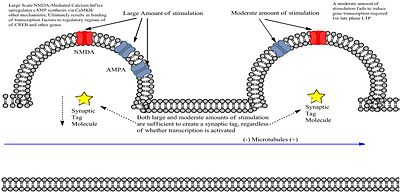
محرک القا کننده L-LTP دو فرآیند مستقل را القا می کند که شامل یک برچسب بیولوژیکی دارینهی است که سیناپس را به عنوان تحریک شده شناسایی می کند و یک رشته ژنومی که mRNA ها و پروتئین های جدید (محصولات انعطاف پذیری) تولید می کند. در حالی که تحریک ضعیف سیناپس ها را نیز نشان می دهد، رشته تولید نمی کند. پروتئین های تولید شده در رشته به طور مشخصی بی قید هستند، زیرا به سیناپس هایی که اخیراً برچسب گذاری شده اند متصل می شوند. با این حال، همانطور که فری و موریس کشف کردند، برچسب موقتی است و اگر پروتئینی برای گرفتن خود را نشان ندهد، ناپدید می شود. بنابراین، اگر قرار است L-LTP توسط تحریک فرکانس بالا القا شود، تولید برچسب و پروتئین باید همپوشانی داشته باشند.
آزمایشی که توسط فری و موریس انجام شد شامل تحریک دو مجموعه مختلف از الیاف جانبی شافر بود که روی یک جمعیت سلولی CA1 سیناپس اعمال میشوند. آنها سپس EPSP میدانی مرتبط با هر محرک را در مسیرهای S1 یا S2 برای تولید E-LTP و L-LTP در سیناپسهای مختلف درون یک نورون ، بر اساس شدت محرک، ثبت کردند. نتایج نشان داد: 1) اینکه E-LTP تولید شده توسط تحریک ضعیف می تواند به L-LTP تبدیل شود اگر یک محرک قوی S2 قبل یا بعد از آن تحویل داده شود و 2) توانایی تبدیل E-LTP به L-LTP با افزایش فاصله بین دو تحریک کاهش یافت که این وابستگی زمانی ایجاد کرد. هنگامی که آنها تلفیق پروتئین را قبل از تحویل تحریک قوی S2 مسدود کردند، از تبدیل به L-LTP جلوگیری شد و اهمیت ترجمه mRNA های تولید شده توسط رشته ژنومی را نشان داد.
تحقیقات بعدی خاصیت دیگری از برچسبگذاری سیناپسی را شناسایی کردند که شامل تعاملات بین L-LTP و LTD دیرهنگام است. این پدیده اولین بار توسط ساجیکومار و فری در سال 2004 شناسایی شد و اکنون بهعنوان "برچسبگذاری متقابل" شناخته میشود. این پدیده شامل تعاملات متقابل بین LTP و LTD در مجموعههای مستقل ورودی سیناپسی است: L-LTP القاشده در یک مجموعه از ورودیهای سیناپسی میتواند E-LTD را به L-LTD در مجموعهای دیگر تبدیل کند. اثر معکوس نیز اتفاق میافتد: E-LTP القاشده در یک سیناپس میتواند به L-LTP تبدیل شود، اگر با یک تحریک القاکننده LTD در سیناپسی مستقل دنبال شود. این پدیده به این دلیل دیده میشود که تلفیق پروتئینهای مرتبط با پلاستیسیته (PRP) غیر اختصاصی توسط L-LTP یا LTD در سیناپس اول برای تبدیل E-LTD/LTP به L-LTD/LTP در سیناپس دوم کافی است، پس از آن که برچسبهای سیناپسی تنظیم شده باشند.
بلیتزر و تیم تحقیقاتی او در سال 2005 اصلاحی را برای این نظریه ارائه کردند و بیان کردند که پروتئین های گرفته شده توسط برچسب سیناپسی در واقع پروتئین های محلی هستند که از mRNA های واقع در دارینه ها ترجمه می شوند. این بدان معناست که mRNA ها محصولی از رشته ژنومی نیستند که توسط یک محرک قوی آغاز شده اند، بلکه در نتیجه رونویسی پایه مستمر تحویل داده می شوند. آنها پیشنهاد کردند که حتی سیناپسهای با تحریک ضعیف که برچسبگذاری شدهاند، میتوانند پروتئینهای تولید شده از یک تحریک قوی در نزدیکی خود را با وجود نداشتن رشته ژنومی بپذیرند.
انتقال mRNA به ستون فقرات دارینهیک و اسکلت سلولی[ویرایش]
تئوری برچسبگذاری سیناپسی/برچسب و تسخیر به طور بالقوه این مساله مهم را توضیح میدهد که چگونه mRNA، پروتئینها و سایر مولکولها ممکن است بهطور خاص به ستونهای دارینهی خاص در طول فاز پایانی LTP منتقل شوند. مدتهاست که مشخص شده است که فاز پایانی LTP به تلفیق پروتئین در ستون فقرات دارینهیک خاص بستگی دارد، که با تزریق آنیزومایسین به ستون فقرات دارینهیک و مشاهده عدم وجود LTP در اخر کار ثابت شده است. [۳] برای دستیابی به ترجمه در ستون فقرات دارینهیک، نورون ها باید mRNA را در هسته تلفیق کنند، آن را در یک کمپلکس ریبونوکلئوپروتئین بسته بندی کنند، انتقال را آغاز کنند، از ترجمه در حین انتقال جلوگیری کنند و در نهایت کمپلکس RNP را به ستون فقرات دارینهیک مناسب تحویل دهند. [۴] این فرآیندها تعدادی قید را در بر می گیرد و برچسب گذاری/برچسب و ضبط سیناپسی نمی تواند همه آنها را توضیح دهد. با این وجود، برچسب زدن سیناپسی احتمالا نقش مهمی در هدایت انتقال mRNA به ستون فقرات دارینهیک مناسب و سیگنال دادن به مجموعه mRNA-RNP برای جدا شدن و ورود به ستون فقرات دارینهیک ایفا می کند.
هویت یک سلول و هویت ساختارهای درون سلولی تا حد زیادی توسط رونوشت های RNA تعیین می شود. با در نظر گرفتن این فرض، نتیجه می شود که رونویسی سلولی، انتقال، و ترجمه mRNA در تعدادی از مقاطع مختلف تغییر می کند. [۵] با شروع رونویسی، مولکول های mRNA به طور بالقوه از طریق پیوند متناوب اگزون ها و اینترون ها اصلاح می شوند. مکانیسمهای پیرایش متناوب به سلولها اجازه میدهد تا مجموعه متنوعی از پروتئینها را از یک ژن واحد در ژنوم تولید کنند. پیشرفتهای اخیر در نسل بعدی توالییابی امکان درک بیشتر تنوع سلولهای یوکاریوتی را از طریق انواع اسپلایس فراهم کرده است. [۶]
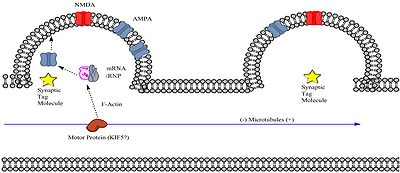
mRNA رونویسی شده باید به ستون فقرات دارینهیک مورد نظر برسد تا ستون فقرات L-LTP را بیان کند. نورون ها ممکن است mRNA را به خارهای دارینهی خاص در یک بسته همراه با یک کمپلکس ریبونوکلئوپروتئین (RNP) انتقال دهند. کمپلکس حمل و نقل RNP یک زیرگروه از گرانول RNA است. گرانول های حاوی دو پروتئین با اهمیت شناخته شده برای پلاستیسیته سیناپسی، CaMKII (کیناز II وابسته به کالمودولین) و ژن اولیه فوری Arc، شناسایی شده اند که با نوعی از پروتئین حرکتی کینزین، KIF5 مرتبط هستند. [۷] علاوه بر این، شواهدی وجود دارد که نشان می دهد mRNA پلی آدنیله با میکروتوبول ها در نورون های پستانداران، حداقل در شرایط آزمایشگاهی، مرتبط است. [۸] از آنجایی که رونوشتهای mRNA قبل از صدور از هسته، تحت پلیآدنیلاسیون قرار میگیرند، این نشان میدهد که mRNA ضروری برای LTP فاز آخر ممکن است قبل از رسیدن به ستون فقرات دارینهیک در امتداد میکروتوبولهای درون شفت دارینهیک حرکت کند.
هنگامی که کمپلکس RNA/RNP از طریق پروتئین حرکتی به ناحیه ای در مجاورت ستون فقرات دارینهیک خاص می رسد، باید به نحوی توسط فرآیندی در ستون فقرات دارینهیک "اسیر" شود. این فرآیند احتمالاً شامل برچسب سیناپسی ایجاد شده توسط تحریک سیناپسی با قدرت کافی است. برچسبگذاری سیناپسی ممکن است منجر به گرفتن کمپلکس RNA/RNP از طریق هر تعداد مکانیسم ممکن از جمله موارد زیر باشد:
- برچسب سیناپسی باعث ورود میکرو لوله شفاف به داخل ستون فقرات دارینهیک می شود. تحقیقات اخیر نشان داده است که میکرولوله ها می توانند به صورت شفاف و وابسته به فعالیت وارد ستون فقرات دارینهیک شوند. [ [۹] ]
- برچسب سیناپسی باعث جدا شدن محموله از پروتئین موتور می شود و به نوعی آن را به ریز رشته های تشکیل شده به صورت پویا هدایت می کند.
تلفیق پروتئین محلی[ویرایش]
از دهه 1980، بیشتر و بیشتر مشخص شد که دارینه ها حاوی ریبوزوم ها ، پروتئین ها و اجزای RNA برای دستیابی به ترجمه محلی و مستقل پروتئین هستند. بسیاری از mRNA های نشان داده شده در دارینه ها، پروتئین هایی را رمزگذاری می کنند که در LTP نقش دارند، از جمله گیرنده AMPA و زیر واحدهای CaMKII، و پروتئین های مرتبط با اسکلت سلولی MAP2 و Arc .
محققان [۱۰] با بررسی توزیع Arc mRNA پس از تحریک انتخابی سیناپسهای خاص یک سلول هیپوکامپ، شواهدی از تلفیق موضعی ارائه کردند. آنها دریافتند که Arc mRNA در سیناپسهای فعال جمع شده است و پروتئین Arc به طور همزمان در آنجا ظاهر میشود. این نشان می دهد که mRNA به صورت محلی ترجمه شده است.
این رونوشتهای mRNA به روشی وابسته به کلاهک ترجمه میشوند، به این معنی که از یک نقطه لنگر "کلاه" برای تسهیل اتصال ریبوزوم به ناحیه ترجمه نشده 5 استفاده میکنند. اعضای گروه 4 فاکتور اغاز یوکاریوتی (eIF4) زیرواحدهای ریبوزومی را به انتهای mRNA جذب میکنند، و مونتاژ مجموعه شروع eIF4F هدف کنترل ترجمه است: فسفوریلاسیون eIF4F درپوش را برای بارگذاری مجدد سریع در معرض دید قرار میدهد و مرحله محدودکننده سرعت ترجمه را تسریع میکند. پیشنهاد می شود که تشکیل کمپلکس eIF4F در طول LTP تنظیم شود تا ترجمه محلی افزایش یابد. علاوه بر این، کمپلکس بیش از حد eIF4F باعث بی ثباتی LTP می شود.
محققان توالی هایی را در mRNA شناسایی کرده اند که مقصد نهایی آن را تعیین می کنند - به نام عناصر محلی سازی (LEs)، کدهای پستی، و عناصر هدف (TEs). اینها توسط پروتئین های اتصال RNA شناسایی می شوند که برخی از نامزدهای بالقوه MARTA و ZBP1 هستند. [۱۱] [۱۲] آنها TE ها را می شناسند و این تعامل منجر به تشکیل کمپلکس های پروتئین ریبونوکلئوتیدی (RNP) می شود که با کمک پروتئین های حرکتی در امتداد رشته های اسکلت سلولی به سمت ستون فقرات حرکت می کند. TE های دارینهیک در ناحیه ترجمه نشده چندین mRNA مانند MAP2 و alphaCaMKII شناسایی شده اند. [۱۳] [۱۴]
مدل های احتمالی برچسبی[ویرایش]
برچسبگذاری سیناپسی احتمالاً شامل کسب مکانیسمهای نگهداری مولکولی توسط یک سیناپس است که پس از آن امکان حفظ تغییرات سیناپسی را فراهم میکند. [۱۵] چندین فرآیند پیشنهادی وجود دارد که از طریق آنها برچسب گذاری سیناپسی عمل می کند. یک مدل نشان می دهد که برچسب اجازه تلفیق پروتئین محلی را در سیناپس مشخص می دهد که سپس منجر به تغییراتی در قدرت سیناپسی می شود. یکی از نمونههای این مکانیسم پیشنهادی، لنگر انداختن mRNA PKMzeta به سیناپس برچسبگذاری شده است. این لنگر سپس فعالیت PKMzeta ترجمه شده، یک پروتئین مهم مرتبط با پلاستیسیته، را در این مکان محدود می کند. یک مدل متفاوت پیشنهاد میکند که تغییرات سیناپسی کوتاهمدت ناشی از محرک، خود یک برچسب هستند. محصولات پروتئینی تحویل داده شده یا ترجمه شده بعدی برای تقویت این تغییر عمل می کنند. به عنوان مثال، حذف گیرندههای AMPA به دلیل تحریک فرکانس پایین که منجر به LTD میشود، توسط یک محصول پروتئینی جدید تثبیت میشود که در سیناپسهایی که درونسازی رخ نداده است، غیرفعال میشود. همانطور که مدل دیگری نشان می دهد، برچسب همچنین می تواند یک ردیابی حافظه پنهان باشد. سپس فعالیت پروتئین ها برای ردیابی حافظه لازم است تا منجر به تغییرات پایدار در قدرت سیناپسی شود. بر اساس این مدل، تغییرات ناشی از ردیابی حافظه نهفته، مانند رشد فیلیپودیای جدید، خود تگ هستند. این برچسب ها به محصولات پروتئینی برای تثبیت، تشکیل سیناپس و تثبیت سیناپس نیاز دارند. در نهایت، مدل دیگری پیشنهاد میکند که محصولات مولکولی مورد نیاز به شاخههای دارینهی مناسب هدایت شوند و سپس سیناپسهای خاص را تحت اصلاح کارایی، با پیروی از گرادیانهای ریزغلظت Ca++ از طریق کانالهای Ca++ که دریچه های وابسته به ولتاژ دارند پیدا کنند. [۱۶]
برچسب گذاری رفتاری[ویرایش]
در حالی که مفهوم فرضیه برچسبگذاری سیناپسی عمدتاً از آزمایشهایی ناشی میشود که تحریک را روی سیناپسها اعمال میکنند، مدل مشابهی را میتوان با در نظر گرفتن فرآیند یادگیری در یک مفهوم رفتاری گستردهتر ایجاد کرد. [۱۷] فابریسیو بالارینی و همکارانش این مدل برچسبگذاری رفتاری را با آزمایش تشخیص شی فضایی، شرطیسازی متنی و بیزاری از طعم شرطی در موشهای با تمرین ضعیف ایجاد کردند. تمرین کاربردی معمولاً فقط منجر به تغییر حافظه کوتاه مدت می شود. با این حال، آنها این تمرین ضعیف را با یک رویداد رفتاری دلخواه و جداگانه که فرض میشود باعث القای تلفیق پروتئین میشود، همراه کردند. هنگامی که دو رویداد رفتاری در یک چارچوب زمانی خاص همراه شدند، آموزش ضعیف برای ایجاد تغییرات مرتبط با کار در حافظه بلند مدت کافی بود. محققان معتقد بودند که آموزش ضعیف منجر به "برچسب یادگیری" می شود. در طول کار بعدی، برش پروتئین ها منجر به تشکیل حافظه بلندمدت برای این برچسب شد. مدل برچسبگذاری رفتاری با مدل برچسبگذاری سیناپسی مطابقت دارد. یک تحریک ضعیف E-LTP را ایجاد می کند که ممکن است به عنوان برچسب مورد استفاده در تبدیل تقویت ضعیف به L-LTP قوی تر و پایدارتر، پس از اعمال تحریک با شدت بالا عمل کند.
مراجع[ویرایش]
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ ۲٫۰ ۲٫۱ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value). خطای یادکرد: برچسب
<ref>نامعتبر؛ نام «frey» چندین بار با محتوای متفاوت تعریف شده است - ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
- ↑ خطای لوآ در پودمان:Citation/CS1/en/Identifiers در خط 47: attempt to index field 'wikibase' (a nil value).
This article "برچسب گذاری سیناپسی" is from Wikipedia. The list of its authors can be seen in its historical and/or the page Edithistory:برچسب گذاری سیناپسی. Articles copied from Draft Namespace on Wikipedia could be seen on the Draft Namespace of Wikipedia and not main one.